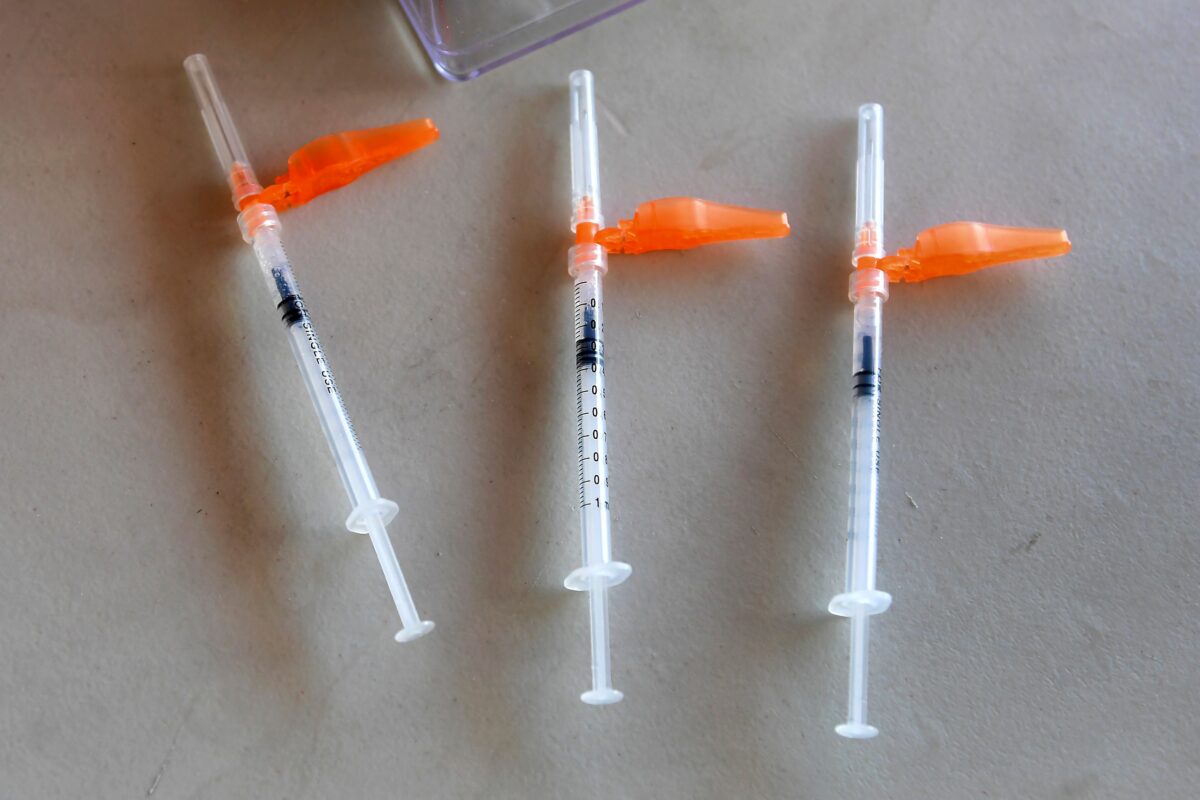
Moderna hoàn thành đơn xin chấp thuận đầy đủ cho vaccine COVID-19
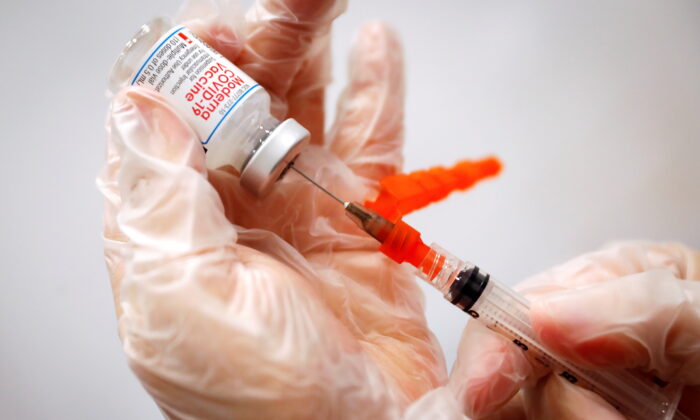
Moderna cho biết họ đã hoàn tất đơn xin chấp thuận đầy đủ vaccine COVID-19 cho các cơ quan quản lý dược phẩm của Hoa Kỳ, trong khi Pfizer và BioNTech đã bắt đầu điền đơn cho liều vaccine COVID-19 bổ sung.
“Đây là lần đệ trình BLA cho vaccine COVID-19 của chúng tôi bắt đầu vào tháng Sáu, là một cột mốc quan trọng trong cuộc chiến của chúng tôi chống lại COVID-19 và với Moderna, đây là lần đệ trình BLA đầu tiên trong lịch sử của công ty chúng tôi,” Stéphane Bancel, Giám đốc điều hành của Moderna, cho biết trong một tuyên bố hôm 25/08, đề cập đến Đơn xin Cấp phép Sinh học (BLA).
Moderna bắt đầu đệ trình các phần của đơn xin phép này vào tháng Sáu; công ty này đã định kỳ gửi thêm dữ liệu cho Cục Quản lý Thực phẩm và Dược phẩm (FDA), bao gồm dữ liệu từ thử nghiệm lâm sàng Giai đoạn 3 với hơn 30,000 người tham gia và được thực hiện với sự hợp tác của Viện Dị ứng và Bệnh truyền nhiễm Quốc gia (NIAID) cùng hai cơ quan khác.
Theo hãng công nghệ sinh học có trụ sở tại Massachusetts này, cuộc thử nghiệm cho thấy vaccine này có hiệu quả 93% trong việc ngăn ngừa lây nhiễm virus Trung Cộng, nguyên nhân gây ra COVID-19.
Các quan chức FDA đã không phúc đáp ngay lập tức yêu cầu bình luận của The Epoch Times.
Việc hoàn tất đơn đăng ký diễn ra sau hai ngày kể từ khi FDA chấp thuận hoàn toàn vaccine Pfizer/BioNTech.
Trong một cuộc gọi với các phóng viên hôm 23/08, một quan chức hàng đầu của FDA đã từ chối cung cấp thông tin chi tiết về đơn xin phép của Moderna. Nhưng quan chức này, Tiến sĩ Peter Marks, đã lưu ý từ khi Pfizer hoàn thành đơn đăng ký đến khi công ty này được chấp thuận hoàn toàn chỉ mất 97 ngày.
Ông Marks cho biết, thời gian này nhanh hơn 40% so với bình thường “để đạt được cột mốc quan trọng này.”
Các quan chức đã xem xét hàng chục nghìn trang dữ liệu về tính an toàn và hiệu quả trước khi chấp thuận hoàn toàn vaccine của Pfizer, bên cạnh những chuyến thăm các cơ sở sản xuất.
Trong khi đó, hôm 25/08, Pfizer và BioNTech cho biết rằng họ đã bắt đầu quy trình Đăng ký Giấy phép Sinh học cho liều thứ ba, hoặc liều bổ sung, cho vaccine của họ.
Đơn đăng ký này được nhiều người xem như một [thủ tục] hình thức sau khi các quan chức y tế thông báo vào đầu tháng này rằng họ sẽ khuyến nghị liều bổ sung cho tất cả người lớn, ngay cả những người khỏe mạnh, sau khi vaccine này được chấp thuận.
Chỉ có ba loại vaccine COVID-19 đã được sử dụng tại Hoa Kỳ kể từ khi căn bệnh này xuất hiện lần đầu tiên ở nước này vào năm ngoái (2020). Cho đến nay, hai loại vaccine sử dụng công nghệ mRNA do Pfizer và Moderna sản xuất, được sử dụng rộng rãi nhất.
Hơn 205 triệu liều Pfizer và hơn 143 triệu liều Moderna đã được sử dụng tính đến 24/08, theo dữ liệu liên bang. Trong khi vaccine Johnson & Johnson được sử dụng là 14 triệu liều.
Không giống như vaccine 1 liều của Johnson & Johnson, vaccine của Pfizer và Moderna được dùng theo phác đồ hai liều; các liều cách nhau vài tuần.
Tuy nhiên, các quan chức y tế gần đây đã thông báo rằng mọi người nên chích liều bổ sung nếu họ đã chích Pfizer hoặc Moderna. Các quan chức cho biết một khuyến nghị tương tự có thể sẽ được đưa ra đối với vaccine một liều của hãng Johnson & Johnson.
Johnson & Johnson chưa nộp Đơn đăng ký Giấy phép Sinh học cho vaccine COVID-19 của mình.
Tiến sĩ Anthony Fauci, người chỉ đạo NIAID, cho biết trên “CBS This Morning” tuần này rằng việc chấp thuận vaccine Moderna và Johnson & Johnson có khả năng không còn “quá xa.”
Ông nói thêm, “Tôi nghĩ đó là vấn đề tạm thời. Tôi không nghĩ rằng có gì khác biệt nhất thiết về quy trình, chỉ là họ đã gửi hoặc đang gửi tài liệu của họ muộn hơn một chút hoặc sau khi Pfizer đã làm điều đó.”
Anh Zachary Stieber phụ trách mảng tin tức Hoa Kỳ, bao gồm cả tin tức chính trị và các vụ kiện ở Hoa Kỳ. Anh bắt đầu làm việc cho The Epoch Times với vai trò là một phóng viên đưa tin về thành phố New York.
Thu Anh biên dịch
Quý vị tham khảo bản gốc từ The Epoch Times
Xem thêm: