FDA: Thuốc huyết áp bị thu hồi vì chứa ‘tạp chất’ gây ung thư tiềm ẩn
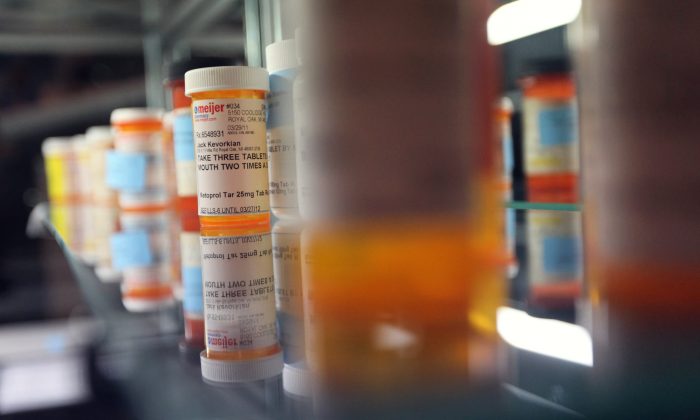
Thuốc huyết áp do Công ty Dược phẩm Lupin sản xuất đang bị Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) thu hồi vì khả năng chứa một tạp chất gây ung thư.
Theo FDA, việc thu hồi tự nguyện này bao gồm các viên nén Irbesartan của công ty này và các viên nén Hydrochlorothiazide ở cấp độ người tiêu dùng.
Cơ quan FDA, trong một thông cáo báo chí hồi tuần trước, cho biết một “chất có thể gây ung thư ở người” đã được phát hiện sau khi có các kết quả thử nghiệm.
Cơ quan này cho biết: “Là một phần trong quá trình đánh giá liên tục của công ty Lupin, phân tích cho thấy một số lô API được thử nghiệm (nhưng không phải lô thành phẩm) chứa N-nitrosoirbesartan, đã vượt quá ngưỡng an toàn theo quy chuẩn đối với tạp chất này”.
Hiện công ty Lupin vẫn chưa nhận được bất kỳ báo cáo nào về bệnh tật có liên quan đến vấn đề này, FDA cho biết.
Nhưng công ty này, hoạt động “hết sức thận trọng”, hiện đang thu hồi tất cả các lô Viên nén Irbesartan ở các liều lượng 75 mg, 150 mg và 300 mg; và lô Viên nén Irbesartan và Hydrochlorothiazide USP ở liều lượng mạnh 150 mg/12.5 mg và 300 mg/12.5mg tại Hoa Kỳ.
Theo FDA, các viên thuốc này được đóng gói trong các chai loại 30-90 (viên) và được phân phối trên toàn quốc cho các đại lý bán buôn, chuỗi nhà thuốc, nhà thuốc đặt hàng qua đường bưu điện, và các siêu thị, vốn bao gồm danh sách số lô và ngày phân phối trong tờ thông báo thu hồi của công ty. Số lô nằm ở mặt bên của chai thuốc.
Công ty Dược phẩm Lupin, một công ty đa quốc gia có trụ sở tại Ấn Độ, đã ngừng hoạt động tiếp thị cho các nhãn thuốc Irbesartan, và Irbesartan và HCTZ vào tháng 01/2021, FDA cho biết. Thuốc này được sử dụng để điều trị tăng huyết áp, hoặc huyết áp cao.
Từ tháng 10/2018 đến hôm 30/09/2021, Công ty Dược phẩm Lupin cho biết họ đã nhận được bốn báo cáo về bệnh tật từ thuốc Irbesartan và không có báo cáo nào từ thuốc Irbesartan và Hydrochlorothiazide.
FDA cũng cho biết: “Viên nén Irbesartan USP là một dạng thuốc ức chế thụ thể angiotensin II được chỉ định để điều trị tăng huyết áp, hạ huyết áp, bệnh thận do đái tháo đường ở bệnh nhân tăng huyết áp mắc bệnh tiểu đường type 2, tăng creatinin huyết thanh và protein niệu.”
Các phản ứng bất lợi hoặc các vấn đề về chất lượng có thể được báo cáo qua chương trình trực tuyến Báo cáo Sự cố Bất lợi MedWatch của FDA hoặc qua đường bưu điện.
Thông báo của FDA cũng lưu ý rằng những người đang sử dụng viên nén Irbesartan hoặc Irbesartan và Hydrochlorothiazide nên tiếp tục làm như vậy đồng thời liên lạc với bác sĩ, dược sĩ hoặc nhà cung cấp của họ về việc họ có nên tìm kiếm phương pháp điều trị thay thế hay không.
Cách đây vài năm, một số công ty dược phẩm của Trung Quốc đã bị FDA cảnh báo do có tạp chất được phát hiện trong các loại thuốc huyết áp khác, dẫn đến các cuộc thu hồi trên diện rộng.
Ông Jack Phillips là một phóng viên về tin tức mới nhất của The Epoch Times có trụ sở tại New York.
Thanh Tâm biên dịch
Quý vị tham khảo bản gốc từ The Epoch Times
Xem thêm: