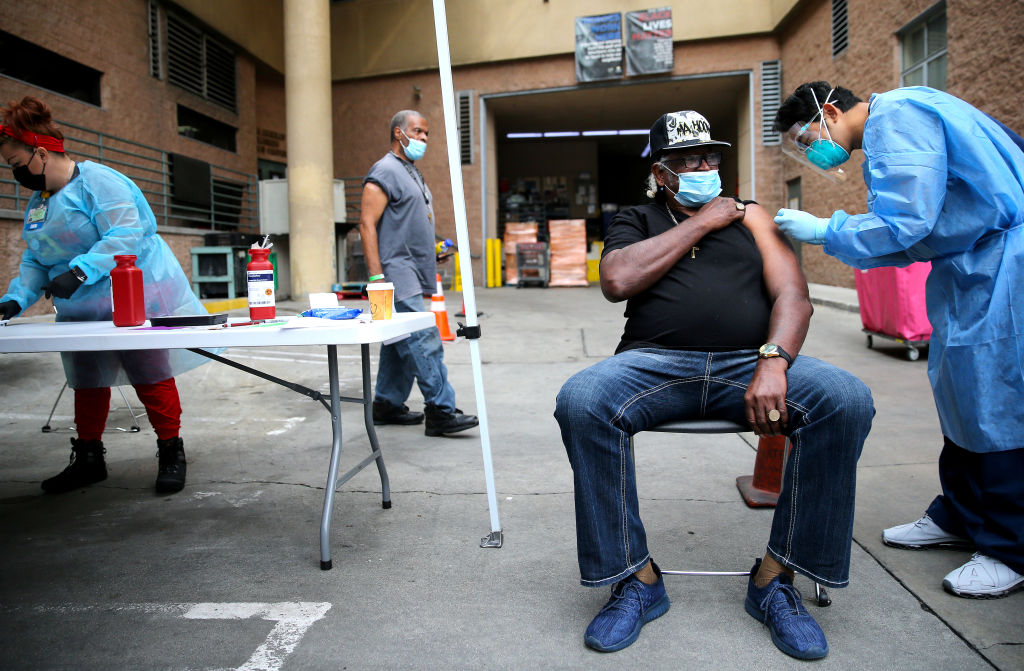
FDA chấp thuận vaccine COVID-19 của Moderna cho tất cả người trưởng thành
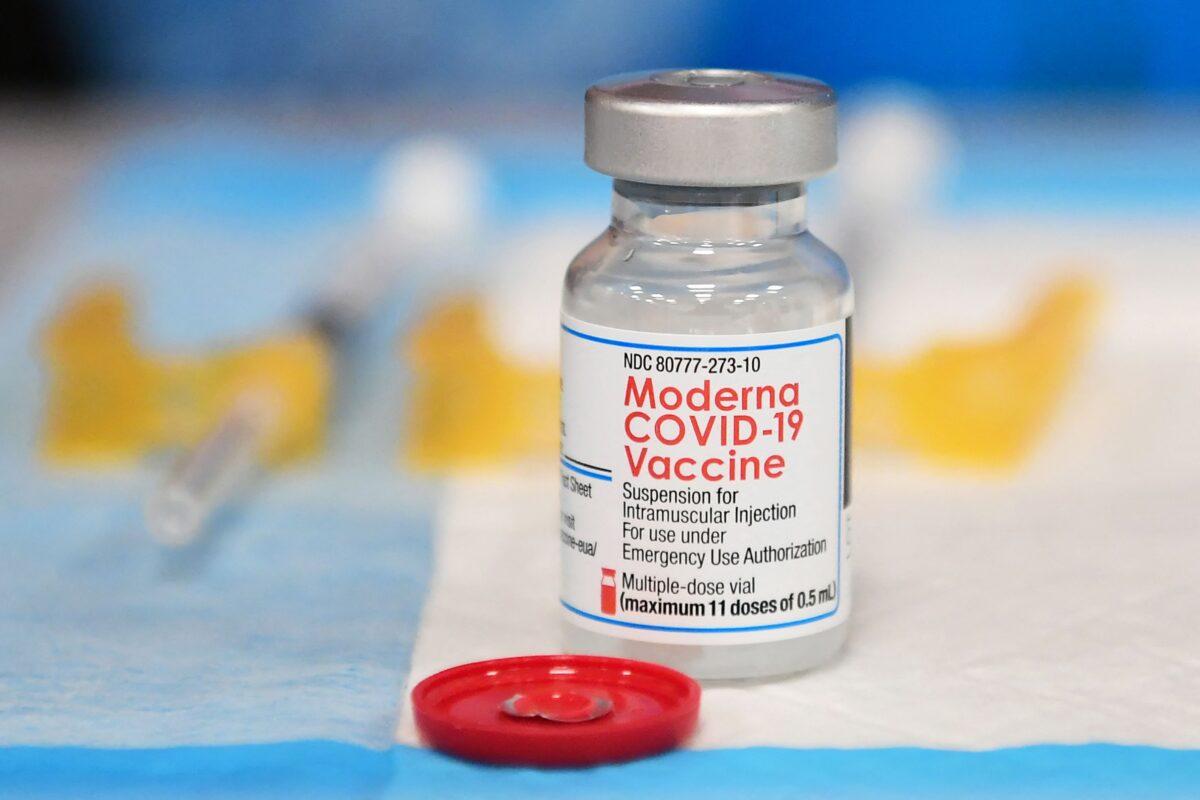
Hôm thứ Hai (31/01), Cơ quan Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) đã chấp thuận vaccine ngừa virus gây ra COVID-19 của Moderna cho tất cả người Mỹ từ 18 tuổi trở lên, mặc dù loại vaccine này cung cấp ít khả năng bảo vệ chống lại bệnh tật kể từ khi xuất hiện biến thể virus Omicron.
FDA cho biết vaccine này có hiệu quả 93% trong việc ngăn ngừa virus Trung Cộng gây ra bệnh COVID-19, hay còn gọi là SARS-CoV-2.
Nhưng dữ liệu được phân tích, vốn cũng cho thấy loại thuốc này có hiệu quả 98% trong việc ngăn ngừa bệnh nặng, đã được thu thập trước khi Omicron xuất hiện.
Biến thể tương đối mới này dễ dàng vượt qua khả năng bảo vệ có được từ loạt mũi chích chính (hai liều) của Moderna và hai loại vaccine COVID-19 khác được sử dụng ở Hoa Kỳ, theo các nghiên cứu và dữ liệu thực tế, bao gồm cả nghiên cứu gần đây được Trung tâm Kiểm soát và Phòng ngừa Dịch bệnh xác nhận.
Tiến sĩ Peter McCullough, một bác sĩ tim mạch tại Trung tâm Y tế Đại học Baylor, cho biết việc chấp thuận này “không có cơ sở chứng minh về mặt lâm sàng cũng như không được hỗ trợ bởi dữ liệu lâm sàng”.
“Chúng ta cần một thử nghiệm ngẫu nhiên lớn trên bệnh nhân Omicron với kết quả tổng hợp của số ca nhập viện và tử vong. Do lịch sử về tính an toàn rất kém của vaccine COVID-19, chúng ta rõ ràng sẽ cần một mối quan hệ lớn hơn giữa lợi ích và nguy cơ trước khi những vaccine này có thể được áp dụng trong thực hành lâm sàng. Với tính chất nhẹ của Omicron và việc quản lý biến thể này dễ dàng, ít có khả năng bất kỳ loại vaccine nào sẽ có vai trò gì đối với biến thể này,” ông nói với The Epoch Times trong một email.
Tiến sĩ Harvey Risch, một giáo sư dịch tễ học tại Trường Y tế Công cộng Yale, nói thêm rằng FDA “lẽ ra phải yêu cầu bằng chứng về Omicron như là một phần trong quá trình cân nhắc của họ, khi mà giờ đây Delta đang suy yếu.”
[Tuy nhiên] Tiến sĩ Thomas Russo, một chuyên gia về các bệnh truyền nhiễm tại Trường Y khoa và Y sinh Jacobs thuộc Đại học Buffalo, không đồng ý với quan điểm này.
Ông nói với The Epoch Times: “Chúng tôi có một lượng lớn dữ liệu hỗ trợ rằng lợi ích là rất lớn và loại vaccine này đặc biệt an toàn. Tôi thực sự hơi ngạc nhiên vì việc chấp thuận mất nhiều thời gian đến vậy nhưng có vẻ như FDA đã làm tất cả công việc cần thiết để bảo đảm rằng mọi thứ đều theo trật tự.”
Một phát ngôn viên của FDA trong một email gửi tới The Epoch Times đã từ chối trả lời khi được hỏi tại sao dữ liệu sau khi có Omicron không được xem xét trước khi chấp thuận và liệu các quan chức có lo ngại về việc vaccine không bảo vệ tốt trước biến thể mới hay không.
FDA cho biết gói mà họ phân tích bao gồm dữ liệu tiền lâm sàng và lâm sàng từ một thử nghiệm Giai đoạn 3 theo dõi khoảng 15,000 người chích vaccine. Dữ liệu này cũng đã được FDA sử dụng để hỗ trợ việc cấp phép sử dụng khẩn cấp cho chính loại vaccine này hồi tháng 12/2020.
Cơ quan này đã phân tích dữ liệu trên để xác định liệu vaccine có đáp ứng các tiêu chuẩn để được chấp thuận hay không.
Vaccine đã được chấp thuận sẽ được bán trên thị trường với tên gọi Spikevax. Nó có công thức tương tự như loại vaccine được cấp phép [sử dụng khẩn cấp] và có thể được sử dụng thay thế cho mũi chích được cấp phép, theo FDA. Spikevax trước đây đã được chấp thuận ở nhiều quốc gia khác, trong đó có Canada, Israel, và Nhật Bản.
“Công chúng có thể yên tâm rằng Spikevax đáp ứng các tiêu chuẩn cao của FDA về độ an toàn, tính hiệu quả và chất lượng sản xuất cần thiết của bất kỳ loại vaccine nào được phép sử dụng ở Hoa Kỳ,” Tiến sĩ Janet Woodcock, quyền giám đốc của cơ quan này cho biết trong một tuyên bố.
Tiến sĩ Peter Marks, Giám đốc Trung tâm Đánh giá và Nghiên cứu Sinh phẩm của FDA cho biết: “Các chuyên gia y tế và khoa học của FDA đã tiến hành đánh giá kỹ lưỡng dữ liệu khoa học và thông tin trong hồ sơ xin chấp thuận liên quan đến độ an toàn, tính hiệu quả, và chất lượng sản xuất của Spikevax.”
Phát ngôn viên của FDA cho biết, tài liệu khái quát về quyết định này, một bản Tóm tắt Cơ sở cho Hành động Điều chỉnh, vẫn chưa được công bố.
Sự chấp thuận chỉ dành cho phác đồ chính của Moderna, bao gồm hai mũi chích được tiêm cách nhau khoảng một tháng.
Theo nghiên cứu về các tác động của biến thể này, phác đồ chính không mang lại lợi ích gì nhiều về mặt bảo vệ chống lại lây nhiễm kể từ khi Omicron trở thành biến thể chiếm ưu thế. Các quan chức y tế liên bang khuyến cáo người dân nên chích mũi bổ sung của Moderna năm tháng sau mũi thứ hai để được bảo vệ tốt hơn chống lại virus Trung Cộng, mặc dù vẫn chưa rõ mũi chích bổ sung này này kéo dài được bao lâu.
Vaccine của Moderna vẫn giữ được khả năng bảo vệ mạnh mẽ chống lại bệnh nặng và nhập viện, đặc biệt là khi có mũi chích bổ sung.
Sản phẩm của Moderna là loại vaccine COVID-19 thứ hai nhận được sự chấp thuận của FDA. Cơ quan này đã chấp thuận vaccine của Pfizer hồi tháng 08/2021.
Ông Stéphane Bancel, giám đốc điều hành của Moderna, cho biết sự chấp thuận này là “một cột mốc quan trọng trong lịch sử của Moderna vì đây là sản phẩm đầu tiên của chúng tôi đạt được giấy phép ở Hoa Kỳ.”
“Chúng tôi rất cảm kích FDA Hoa Kỳ vì đã xem xét kỹ lưỡng hồ sơ xin chấp thuận của chúng tôi. Chúng tôi cảm thấy khiêm nhường trước vai trò mà Spikevax đang thực hiện để giúp chấm dứt đại dịch này,” ông nói thêm.
Ông Zachary Stieber phụ trách mảng tin tức Hoa Kỳ và các bài viết liên quan đến đại dịch COVID-19. Ông sống tại Maryland.
Minh Ngọc biên dịch
Quý vị tham khảo bản gốc từ The Epoch Times
Xem thêm: